El comisionado de la Agencia Federal de Alimentos y Medicamentos (FDA, por sus siglas en inglés) Stephen Hahn M.D. declaró el jueves que “Durante casi 11 meses, todos hemos estado aprendiendo a vivir y funcionar en un estado de incertidumbre, ajustándonos a una “nueva normalidad”, ya que la pandemia de COVID-19 ha afectado drásticamente la forma en que la mayoría de nosotros vivimos y también ha cobrado vidas trágicamente. de cientos de miles de estadounidenses.
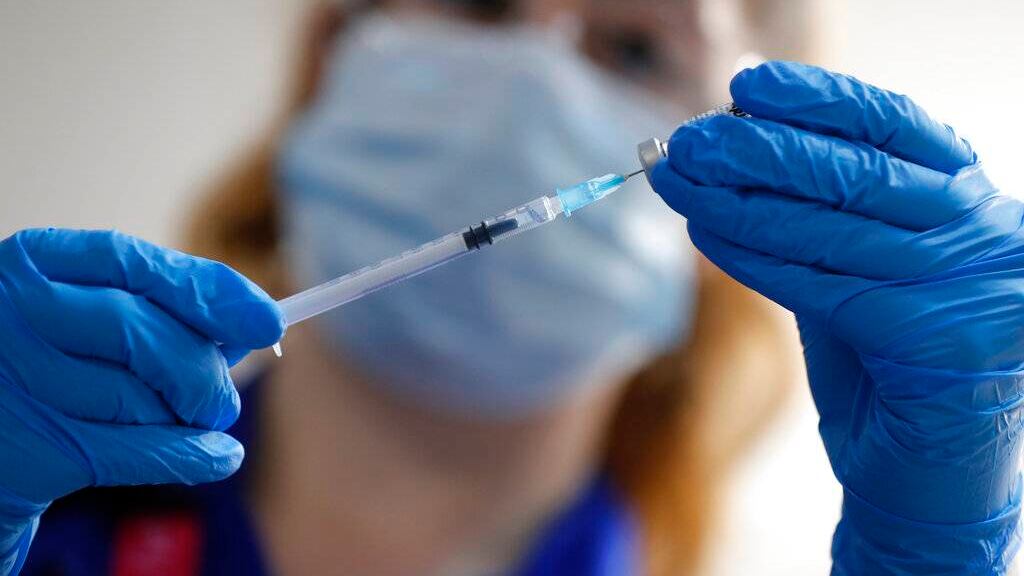
Reconocemos la necesidad urgente de contramedidas médicas para diagnosticar, tratar y prevenir este nuevo virus y hemos estado trabajando diligentemente para facilitar su desarrollo y disponibilidad. En particular, la FDA ha estado trabajando incansablemente con los sectores público y privado para facilitar el rápido desarrollo de las vacunas COVID-19 sin sacrificar nuestros rigurosos estándares científicos de seguridad y eficacia.
Hoy, el Comité Asesor de Vacunas y Productos Biológicos Relacionados (VRBPAC) de la FDA, compuesto por científicos independientes y expertos en salud pública de todo el país, se reúne para discutir la primera solicitud de autorización de uso de emergencia (EUA) de una vacuna para COVID-19. prevención, presentado por Pfizer Inc. en asociación con BioNTech Manufacturing GmbH.
La FDA reconoce que la transparencia y el diálogo son fundamentales para generar confianza pública en las vacunas COVID-19. Una discusión abierta con este comité, disponible para la vista del público y con aportes del público, sobre la totalidad de la evidencia científica con respecto a la seguridad y eficacia de la vacuna de Pfizer y BioNTech ayudará a garantizar una clara comprensión pública de los datos científicos y la información que la FDA evalúa tomar una decisión sobre la autorización de una vacuna para uso de emergencia para la prevención de COVID-19.
El personal de carrera de la FDA, compuesto por médicos, biólogos, químicos, epidemiólogos, estadísticos y otros profesionales, ha estado trabajando las veinticuatro horas del día para evaluar minuciosamente los datos y la información en la solicitud de EUA, para esta posible vacuna COVID-19, en un y una manera basada en la ciencia. Puedo asegurarles que no se autorizará el uso de ninguna vacuna en los Estados Unidos hasta que los funcionarios de carrera de la FDA se sientan seguros de permitir que sus propias familias la reciban.
La FDA se considera el regulador “estándar de oro” de los productos médicos. El proceso que la FDA usa para revisar es respetado en todo el mundo debido a una historia bien establecida que la FDA tiene entre los procesos de revisión más rigurosos y precisos a nivel mundial. Normalmente, el proceso de revisión de las vacunas estudiadas en decenas de miles de personas lleva meses.
Aunque el proceso se ha acelerado en asociación con la revisión de este EUA, el personal de revisión de expertos de la FDA ha revisado miles de páginas de información técnica. Estos datos incluyen, pero no se limitan a, datos de ensayos clínicos, datos no clínicos sobre el desarrollo de la vacuna en el laboratorio y datos de fabricación sobre cómo se fabrica la vacuna. Los funcionarios de carrera de la FDA han estado revisando los datos y la información antes de la reunión del comité asesor público para asegurar una discusión sólida con los expertos independientes.
La reunión de hoy es un paso importante en el proceso, ya que brinda a los expertos científicos externos la oportunidad de brindar valiosos consejos y aportes para que la agencia los considere como parte de su revisión final. Es importante destacar que los funcionarios de carrera de la FDA en el Centro de Evaluación e Investigación Biológica tomarán las decisiones finales sobre la autorización de una vacuna para uso de emergencia.
Después de la reunión del VRBPAC, el personal de carrera de la FDA tomará en cuenta los comentarios del comité mientras continúan su revisión de la solicitud de EUA para determinar si ha cumplido con los estándares de seguridad y efectividad para la emisión de un EUA, así como también para refinar las instrucciones de uso. y los materiales informativos que se proporcionarán a quienes reciban la vacuna.
En este momento de gran urgencia, el personal de la FDA siente la responsabilidad de avanzar lo más rápido posible a través del proceso de revisión. Sin embargo, saben que deben cumplir con su mandato de proteger la salud pública y garantizar que cualquier vacuna autorizada cumpla con nuestros rigurosos estándares de seguridad y eficacia que el pueblo estadounidense espera.
Toda la FDA, incluido yo mismo, mantiene su compromiso de mantener al público informado sobre la evaluación de los datos de una posible vacuna COVID-19, para que una vez disponible, los estadounidenses puedan tener confianza en recibir la vacuna para sus familias y para ellos mismos.
La FDA, una agencia del Departamento de Salud y Servicios Humanos de los Estados Unidos, protege la salud pública al garantizar la seguridad, la eficacia y la seguridad de los medicamentos, vacunas y otros productos biológicos para uso humano y veterinarios, y dispositivos médicos. La agencia también es responsable de la seguridad y protección del suministro de alimentos, cosméticos, suplementos dietéticos, productos que emiten radiación electrónica y de regular los productos de tabaco de nuestra nación”.