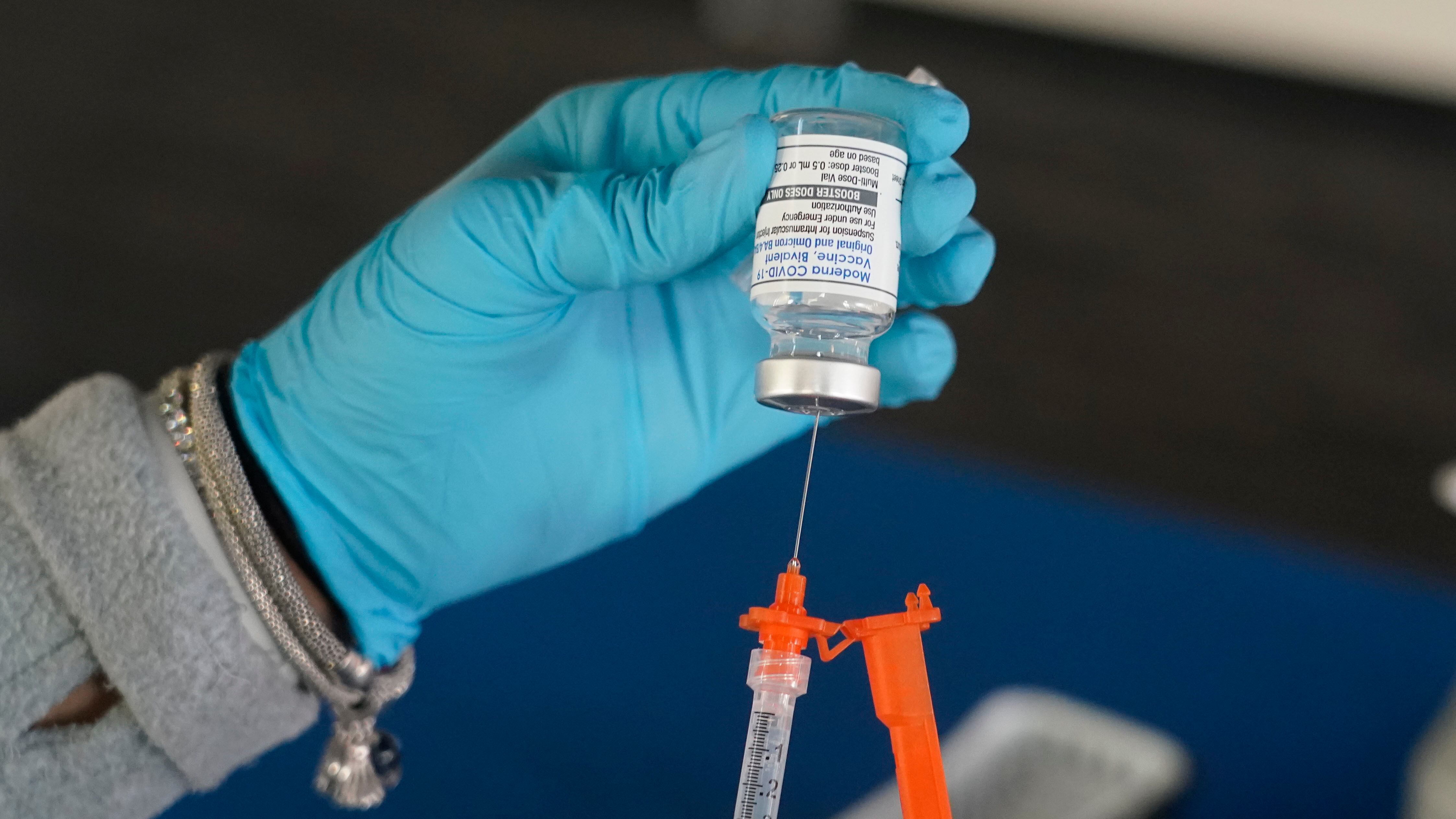
La Administración de Drogas y Alimentos de Estados Unidos modificó el jueves las autorizaciones de uso de emergencia (EUA) de las vacunas Moderna (bivalente) actualizadas y Pfizer-BioNTech COVID-19 para incluir el uso en niños de hasta 6 meses.
“Ahora más niños tienen la oportunidad de actualizar su protección contra el COVID-19 con una vacuna bivalente contra el COVID-19, y alentamos a los padres y cuidadores de aquellos elegibles a que consideren hacerlo, especialmente a medida que nos acercamos a las vacaciones y los meses de invierno, donde más tiempo se gastarán en el interior”, dijo el comisionado de la FDA, Robert Califf, M.D. en declaraciones escritas.
PUBLICIDAD
“A medida que este virus ha cambiado y la inmunidad de la vacunación anterior contra el COVID-19 disminuye, cuantas más personas se mantengan al día con las vacunas contra el COVID-19, más beneficio habrá. será para las personas, las familias y la salud pública al ayudar a prevenir enfermedades graves, hospitalizaciones y muertes”, añadió.
Lo que los padres y cuidadores deben saber:
Los niños de 6 meses a 5 años de edad que recibieron la vacuna Moderna COVID-19 original (monovalente) ahora son elegibles para recibir un refuerzo único de la vacuna Moderna COVID-19 actualizada (bivalente) dos meses después de completar una serie primaria con Moderna monovalente Vacuna para el COVID-19.
Los niños de 6 meses a 4 años de edad que aún no han comenzado su serie primaria de tres dosis de la vacuna Pfizer-BioNTech COVID-19 o aún no han recibido la tercera dosis de su serie primaria ahora recibirán la vacuna actualizada (bivalente) Pfizer- La vacuna BioNTech COVID-19 como la tercera dosis en su serie primaria después de dos dosis de la vacuna original (monovalente) Pfizer-BioNTech COVID-19.
Los niños de 6 meses a 4 años de edad que ya hayan completado su serie primaria de tres dosis con la vacuna original (monovalente) Pfizer-BioNTech COVID-19 no serán elegibles para una dosis de refuerzo de una vacuna bivalente actualizada en este momento. Se esperaría que los niños en este grupo de edad que ya completaron su serie primaria aún tuvieran protección contra los resultados más graves de la variante omicron que circula actualmente. Los datos para respaldar la administración de una dosis de refuerzo bivalente actualizada para estos niños se esperan para enero. La agencia se compromete a evaluar esos datos lo más rápido posible.
PUBLICIDAD
Las vacunas bivalentes COVID-19 de Moderna y Pfizer-BioNTech incluyen un componente de ARNm correspondiente a la cepa original para proporcionar una respuesta inmune que es ampliamente protectora contra COVID-19 y un componente de ARNm correspondiente a los linajes BA.4 y BA.5 de la variante omicron para brindar una mejor protección contra el COVID-19 causado por la variante omicron.
Las personas que reciben las vacunas actualizadas (bivalentes) pueden experimentar efectos secundarios similares informados por personas que recibieron dosis anteriores de las vacunas COVID-19 de ARNm originales (monovalentes).
Las hojas informativas de las vacunas bivalentes contra el COVID-19 para receptores y cuidadores y para proveedores de atención médica incluyen información sobre los posibles efectos secundarios, así como los riesgos de miocarditis y pericarditis.
“Las vacunas siguen siendo la mejor defensa contra las consecuencias más devastadoras de la enfermedad causada por la variante omicron que circula actualmente, como la hospitalización y la muerte. Según los datos disponibles, se espera que las vacunas bivalentes actualizadas brinden una mayor protección contra el COVID-19″, dijo Peter Marks, M.D., Ph.D., director del Centro de Evaluación e Investigación Biológica de la FDA. “Los padres y cuidadores pueden estar seguros de que la FDA ha tenido mucho cuidado en nuestra revisión, y alentamos a los padres de niños de cualquier edad que son elegibles para la vacunación primaria o una dosis de refuerzo de la vacuna bivalente COVID-19 a considerar vacunarse ahora ya que potencialmente puede ayudar a protegerlos de COVID-19 durante un momento en que los casos están aumentando”.
Vacuna Moderna COVID-19, Bivalente
La vacuna monovalente Moderna COVID-19 está autorizada como una serie primaria de dos dosis en personas de seis meses de edad y mayores y como una tercera dosis de serie primaria para personas de 6 meses de edad y mayores que se ha determinado que tienen ciertos tipos de inmunodepresión. Con la autorización de hoy, la vacuna Moderna COVID-19, bivalente ahora está autorizada para su administración en personas de 6 meses a 5 años de edad como una dosis de refuerzo única al menos 2 meses después de completar la vacunación primaria con la vacuna monovalente Moderna COVID-19. La vacuna Moderna COVID-19, bivalente también está autorizada para su uso en personas mayores de 6 años como dosis de refuerzo única al menos dos meses después de completar la vacunación primaria con cualquier vacuna COVID-19 autorizada o aprobada, o recibir la vacuna más reciente. dosis de refuerzo con cualquier vacuna monovalente COVID-19 autorizada o aprobada.
Para la autorización de una sola dosis de refuerzo de la vacuna Moderna COVID-19, bivalente para niños de 6 meses a 5 años de edad, la FDA se basó en datos de respuesta inmunitaria que había evaluado previamente a partir de un estudio clínico en adultos de una dosis de refuerzo de la vacuna COVID-19 bivalente en investigación de Moderna que contenía un componente correspondiente a la cepa original de SARS-CoV-2 y un componente correspondiente al linaje omicron BA.1.
Además, la FDA realizó un análisis de datos de un estudio clínico que comparó la respuesta inmunitaria entre 56 participantes del estudio de 17 meses a 5 años de edad que recibieron una dosis única de refuerzo de la vacuna monovalente Moderna COVID-19 al menos seis meses después de completar una serie primaria de dos dosis de la vacuna para la respuesta inmunitaria entre aproximadamente 300 participantes del estudio de 18 a 25 años de edad que habían recibido una serie primaria de dos dosis de la vacuna monovalente Moderna COVID-19 en un estudio anterior que determinó que la vacuna era eficaz en la prevención del COVID-19. La respuesta inmunitaria a la dosis de refuerzo de la vacuna monovalente Moderna COVID-19 en el grupo de edad de 17 meses a 5 años fue comparable a la respuesta inmunitaria a la serie primaria de dos dosis en los participantes adultos.
La seguridad de una sola dosis de refuerzo de la vacuna Moderna COVID-19, bivalente para niños de 6 meses a 5 años de edad está respaldada por datos de seguridad de un estudio clínico que evaluó una dosis de refuerzo de la vacuna bivalente experimental COVID-19 de Moderna (original y omicron BA.1), datos de seguridad de ensayos clínicos que evaluaron la vacunación primaria y de refuerzo con la vacuna monovalente Moderna COVID-19, y los datos de seguridad posteriores a la comercialización con la vacuna monovalente Moderna COVID-19 y la vacuna Moderna COVID-19, bivalente.
En un estudio clínico, se evaluó la seguridad de una dosis de refuerzo única de la vacuna Moderna COVID-19 monovalente en 145 participantes del estudio clínico de 6 meses a 5 años de edad que recibieron una dosis de refuerzo de la vacuna Moderna COVID-19 monovalente al menos seis meses después finalización de la serie primaria de dos dosis de la vacuna monovalente Moderna COVID-19. Los efectos secundarios informados con mayor frecuencia después de una dosis de refuerzo de la vacuna monovalente Moderna COVID-19 en este grupo de edad incluyeron dolor, enrojecimiento e hinchazón en el lugar de la inyección, hinchazón/sensibilidad de los ganglios linfáticos del brazo o muslo inyectado y fiebre. En los participantes del estudio clínico de 17 a 36 meses de edad, otros efectos secundarios comúnmente informados incluyeron irritabilidad/llanto, somnolencia y pérdida de apetito. En los participantes de ensayos clínicos de 37 meses a 5 años de edad, otros efectos secundarios comúnmente informados incluyeron fatiga, dolor de cabeza, dolor muscular, dolor en las articulaciones, escalofríos y náuseas/vómitos.
Los datos acumulados con la vacuna Moderna bivalente COVID-19 en investigación (original y omicron BA.1) y con la vacuna Moderna COVID-19 monovalente son relevantes para la vacuna Moderna COVID-19, bivalente porque estas vacunas se fabrican utilizando el mismo proceso.
Vacuna Pfizer-BioNTech COVID-19, bivalente
Con la autorización de hoy, los niños de 6 meses a 4 años de edad que aún no hayan recibido la tercera dosis de la serie primaria de tres dosis con la vacuna monovalente Pfizer-BioNTech COVID-19 ahora recibirán la vacuna bivalente Pfizer-BioNTech COVID-19 como la tercera dosis de la serie primaria. La vacuna bivalente contra el COVID-19 de Pfizer-BioNTech también está autorizada para su administración en personas mayores de 5 años como dosis de refuerzo única al menos dos meses después de completar la vacunación primaria con cualquier vacuna contra el COVID-19 autorizada o aprobada, o de recibir de la dosis de refuerzo más reciente con cualquier vacuna COVID-19 monovalente autorizada o aprobada.
Con la acción de hoy, la vacuna monovalente Pfizer-BioNTech COVID-19 ya no está autorizada para su uso como la tercera dosis de la serie primaria de tres dosis en niños de 6 meses a 4 años de edad. La vacuna monovalente Pfizer-BioNTech COVID-19 sigue autorizada para su administración como las dos primeras dosis de la serie primaria de tres dosis en personas de 6 meses a 4 años de edad, como serie primaria de dos dosis para personas de 5 años de edad y mayores. , y como una tercera dosis de serie primaria para personas de 5 años de edad y mayores que se ha determinado que tienen ciertos tipos de compromiso inmunológico.
Se respalda la autorización de la vacuna bivalente contra el COVID-19 de Pfizer-BioNTech para su administración como la tercera dosis de una serie primaria de tres dosis después de dos dosis de la vacuna monovalente contra el COVID-19 de Pfizer-BioNTech en niños de 6 meses a 4 años de edad. por los análisis previos de la FDA de la efectividad de la vacunación primaria con la vacuna monovalente Pfizer-BioNTech COVID-19 en personas de 16 años de edad y mayores y en personas de 6 meses a 4 años de edad, y análisis previos de datos de respuesta inmunitaria en adultos mayores de 55 años de edad que habían recibido una serie primaria de dos dosis y una dosis de refuerzo con la vacuna monovalente Pfizer-BioNTech COVID-19 y una segunda dosis de refuerzo con la vacuna experimental Pfizer-BioNTech bivalente COVID-19 (original y omicron BA.1 ).
La seguridad de la La vacuna bivalente contra el COVID-19 de Pfizer-BioNTech para administrar como la tercera dosis de una serie primaria de tres dosis después de dos dosis de la vacuna monovalente contra el COVID-19 de Pfizer-BioNTech en niños de 6 meses a 4 años de edad se basa en datos de seguridad de un estudio clínico que evaluó una dosis de refuerzo de la vacuna COVID-19 bivalente en investigación de Pfizer-BioNTech (original y omicron BA.1) en personas mayores de 55 años, datos de seguridad de ensayos clínicos que evaluaron la vacunación primaria en personas de 6 meses de edad y mayores con la vacuna monovalente Pfizer-BioNTech COVID-19, datos de seguridad de ensayos clínicos que evaluaron la vacunación de refuerzo en personas de 5 años de edad y mayores con la vacuna monovalente Pfizer-BioNTech COVID-19 y datos de seguridad posteriores a la comercialización con la monovalente Pfizer-BioNTech Vacuna contra el COVID-19 y vacuna contra el COVID-19 de Pfizer-BioNTech, bivalente.
Los datos acumulados con la vacuna bivalente COVID-19 de Pfizer-BioNTech en investigación (original y omicron BA.1) y con la vacuna monovalente Pfizer-BioNTech COVID-19 son relevantes para la vacuna bivalente Pfizer-BioNTech COVID 19 porque estas vacunas se fabrican utilizando el mismo proceso.
Las enmiendas a los EUA se emitieron a Moderna TX Inc. y Pfizer Inc.